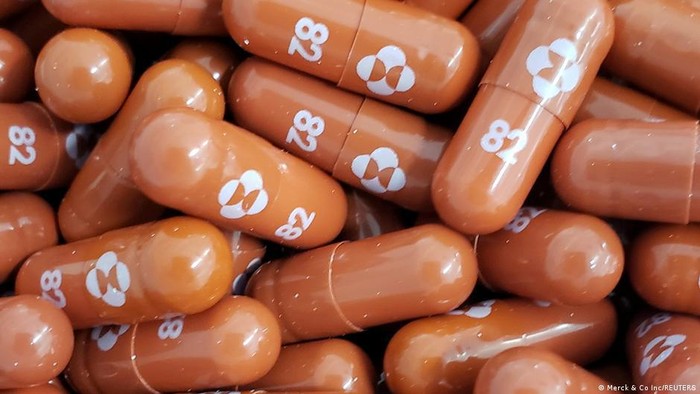
Medicines Patent Pool (MPP) dan PT Kimia Farma Tbk, mengumumkan penandatanganan perjanjian untuk memfasilitasi akses global yang terjangkau untuk Molnupiravir. Berdasarkan ketentuan perjanjian antara Merck, Sharp & Dohme (MSD) dan MPP, melalui lisensi yang diberikan oleh MSD, MPP diizinkan untuk melisensikan lebih lanjut kepada Kimia Farma.
Melansir keterangan tertulis perusahaan, Jumat (21/1/2022), perjanjian ini akan membantu menciptakan akses luas untuk penggunaan Molnupiravir di 105 negara untuk pemenuhan kebutuhan salah satunya adalah di Indonesia dan beberapa negara tujuan lainnya.
Molnupiravir dikembangkan di Universitas Emory dan dilisensikan ke Ridgeback Biotherapeutics oleh Drug Innovation Ventures di Emory (DRIVE), LLC, yang dibentuk oleh Emory untuk memajukan pengembangan kandidat obat tahap awal untuk penyakit virus yang menjadi perhatian global.
SCROLL TO CONTINUE WITH CONTENT
Kerjasama sublisensi dengan Medicines Patent Pool (MPP) adalah suatu terobosan untuk Kimia Farma sebagai industri farmasi Indonesia. Ini adalah langkah penting untuk
meningkatkan akses obat esensial yang masih dalam paten khususnya Molnupiravir, sehingga dapat diakses masyarakat Indonesia dan negara lain. Penandatangan perjanjian ini juga akan mendukung transformasi dan aksesibilitas kesehatan di Indonesia.
Molnupiravir sedang diteliti oleh Merck & Ridgeback untuk pengobatan penyakit Coronavirus ringan hingga sedang 2019 (COVID-19) pada orang dewasa dengan tes diagnostik SARSCoV-2 positif dan yang berisiko tinggi untuk berkembang menjadi COVID-19 yang parah, termasuk rawat inap atau kematian.
Molnupiravir telah diizinkan untuk digunakan di Inggris dan USA. FDA sedang meninjau aplikasi Merck untuk Otorisasi Penggunaan Darurat. Pengajuan didasarkan pada hasil positif dari analisa sementara yang direncanakan dari studi fase 3 MOVe-OUT, studi global Fase 3, teracak, placebo yang terkontrol, studi buta ganda, studi multi-situs dari pasien dewasa yang tidak dirawat di rumah sakit dengan konfirmasi laboratorium COVID-19 ringan hingga sedang dan setidaknya satu faktor risiko untuk berkembang menjadi penyakit parah atau kematian.
(das/dna)